Validation préclinique : en cours
Capacité de production conforme aux BPF : 2028
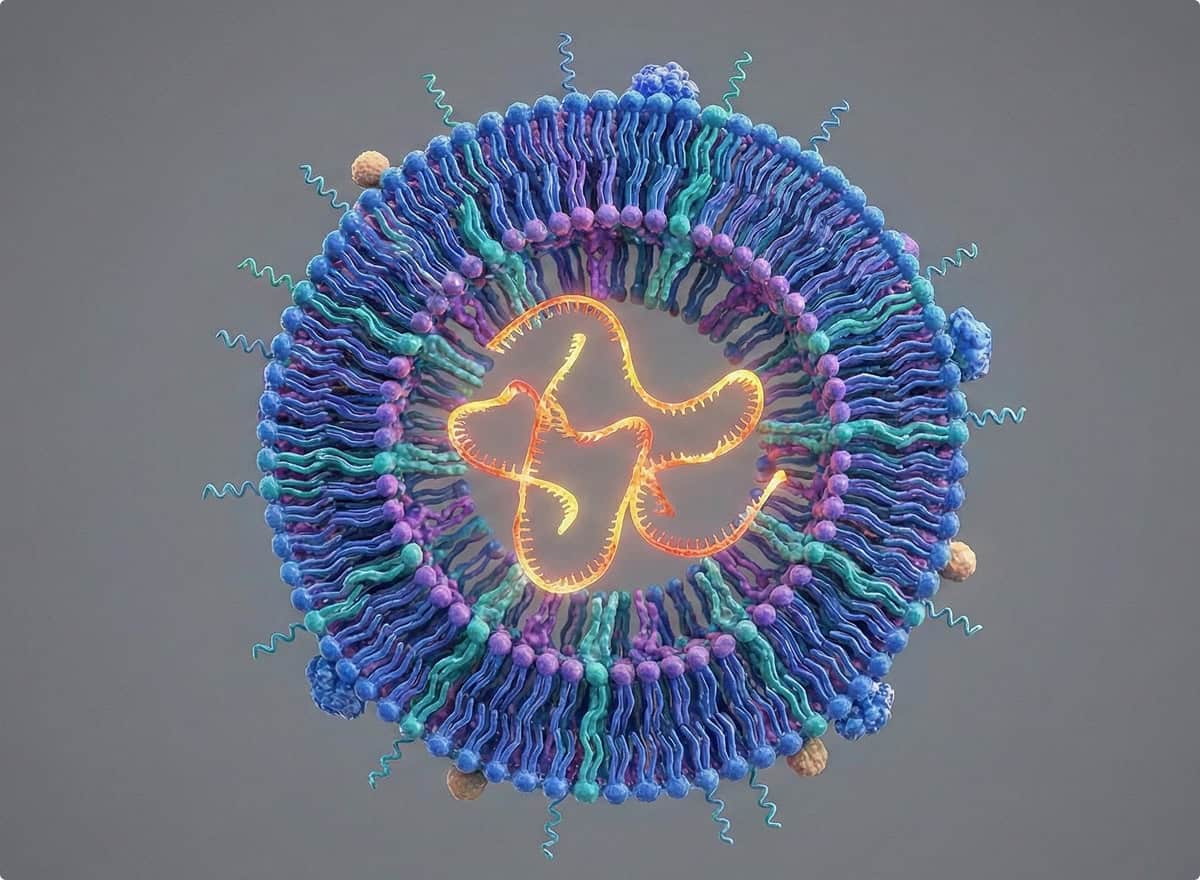
La thérapie SMA de LNPureTx repose sur une nouvelle génération de nanoparticules lipides-polymères (LNP hybrides) permettant la délivrance efficace et sûre d’ARNm codant la protéine SMN. Cette approche vise à remplacer le gène SMN1 déficient par une production endogène directe de la protéine manquante, sans utiliser de vecteurs viraux. Les LNP développés par LNPureTx sont conçus pour être non immunogènes, non inflammatoires et dépourvus de toxicité systémique mesurable, offrant une alternative plus sûre aux thérapies géniques virales actuelles.

Injectables par voie intrathécale, ces LNP atteignent les motoneurones du rachis de façon ciblée, assurant une expression robuste de SMN là où elle est essentielle pour prévenir la dégénérescence neuromusculaire. Leur architecture hybride lipide-polymère offre une capacité d’encapsulation 5 à 10 fois supérieure à celle des vectorisations virales AAV, permettant d’administrer une dose thérapeutique complète en une seule injection à la naissance. Cette puissance de charge ouvre la voie à un traitement réellement compatible avec les formes les plus sévères de la maladie, y compris la SMA de type 1 diagnostiquée néonatalement.
Les LNP de LNPureTx présentent également une stabilité accrue, garantissant une délivrance homogène de l’ARNm et une expression prolongée de SMN.
Leur caractère non viral élimine les risques associés aux anticorps neutralisants anti-AAV, à la saturation de la protéasome capsidique ou aux réactions inflammatoires post-injection. Enfin, le procédé de fabrication de ces LNP hybrides permet une production plus simple, mieux contrôlée et significativement moins coûteuse, avec l’objectif de proposer une thérapie SMA définitive à un coût total inférieur à un million d’euros, contre 2 à 3 millions pour les traitements actuels.
G râce à la combinaison unique de sécurité, stabilité, capacité de charge et accessibilité économique, la thérapie LNP-ARNm de LNPureTx ambitionne de devenir la solution de référence mondiale pour restaurer la protéine SMN et traiter durablement la SMA.
Validation préclinique : en cours
Capacité de production conforme aux BPF : 2028
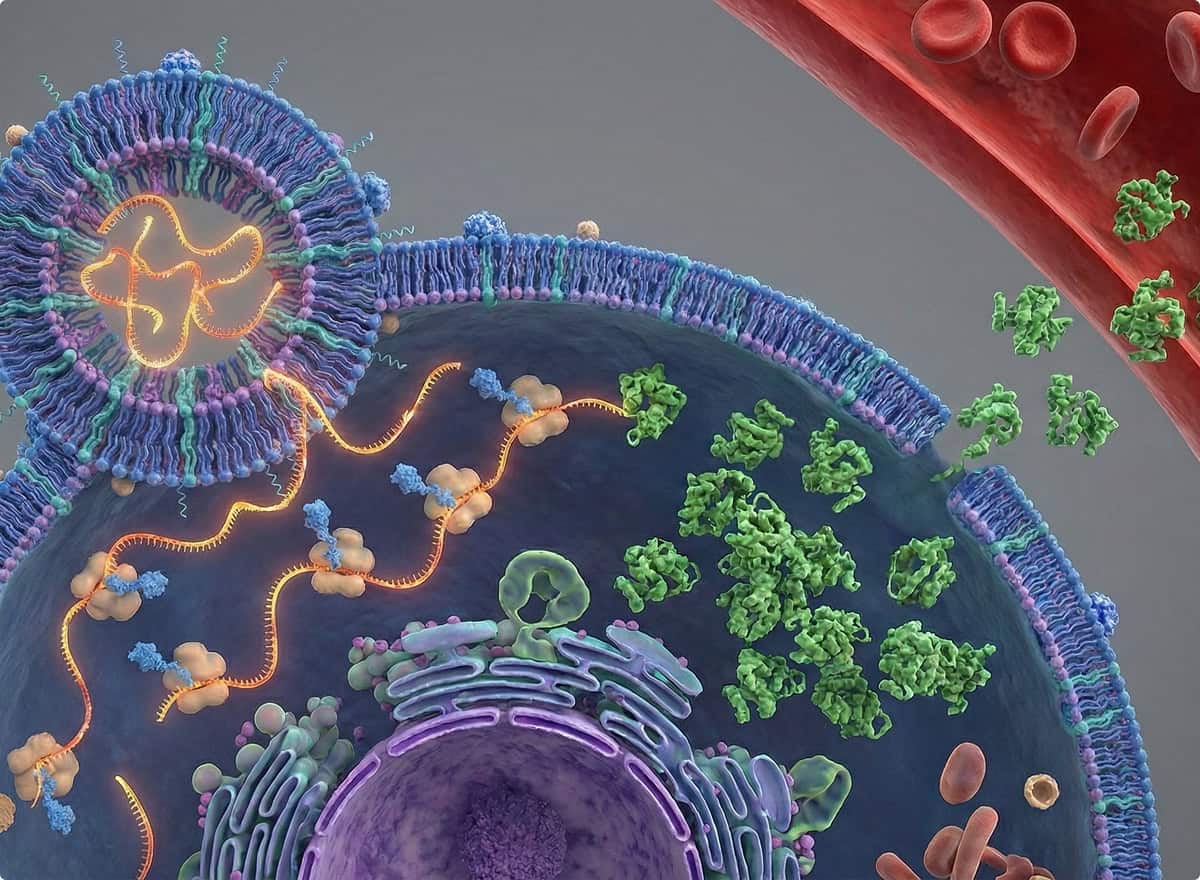
La thérapie développée par LNPureTx pour la NASH repose sur une stratégie innovante : restaurer la production hépatique de la protéine SMN grâce à un ARNm optimisé délivré directement aux hépatocytes. En ciblant la fonction cellulaire altérée par l’absence de SMN1, cette approche permet d’agir en amont des mécanismes pathogéniques de la NASH, y compris l’inflammation chronique, la stéatose et la fibrose progressive. Contrairement aux thérapies géniques virales, LNPureTx s’appuie sur des nanoparticules non virales, non immunogènes et non inflammatoires, permettant des administrations répétées tout au long de la vie, adaptées à une maladie chronique d’évolution lente comme la NASH.

Pour cette indication, LNPureTx a conçu une formulation LNP hybride spécifique pour l’administration portale directe, optimisée pour la stabilité dans un environnement hépatique exigeant. Cette formulation lipide-polymère présente une grande robustesse, protège efficacement l’ARNm et assure sa libération ciblée en quantités particulièrement élevées dans les hépatocytes. Les données précliniques in vivo sur modèles murins montrent une délivrance massive, reproductible et homogène de l’ARNm au sein du parenchyme hépatique, accompagnée d’une expression prolongée et efficace de la protéine SMN.
L’utilisation de LNP non viraux rend possible un schéma thérapeutique répétitif, indispensable pour une pathologie métabolique chronique : absence de réponses immunitaires neutralisantes, tolérance excellente, flexibilité de dose, et possibilité d’adapter le traitement au stade d’évolution de la maladie.
Grâce à leur stabilité renforcée et à leur capacité d’encapsulation très supérieure aux vecteurs AAV, ces LNP permettent une expression de SMN à des niveaux physiologiquement pertinents dans le foie, ouvrant la voie à un véritable contrôle à long terme de la maladie.
En réunissant ciblage hépatique, administration portale, sécurité optimale et expression robuste de SMN, la technologie de LNPureTx vise à établir la première approche ARNm-LNP capable de traiter durablement la NASH liée au déficit en SMN1 et d’enrayer sa progression sur toute la durée de vie des patients.
En développement
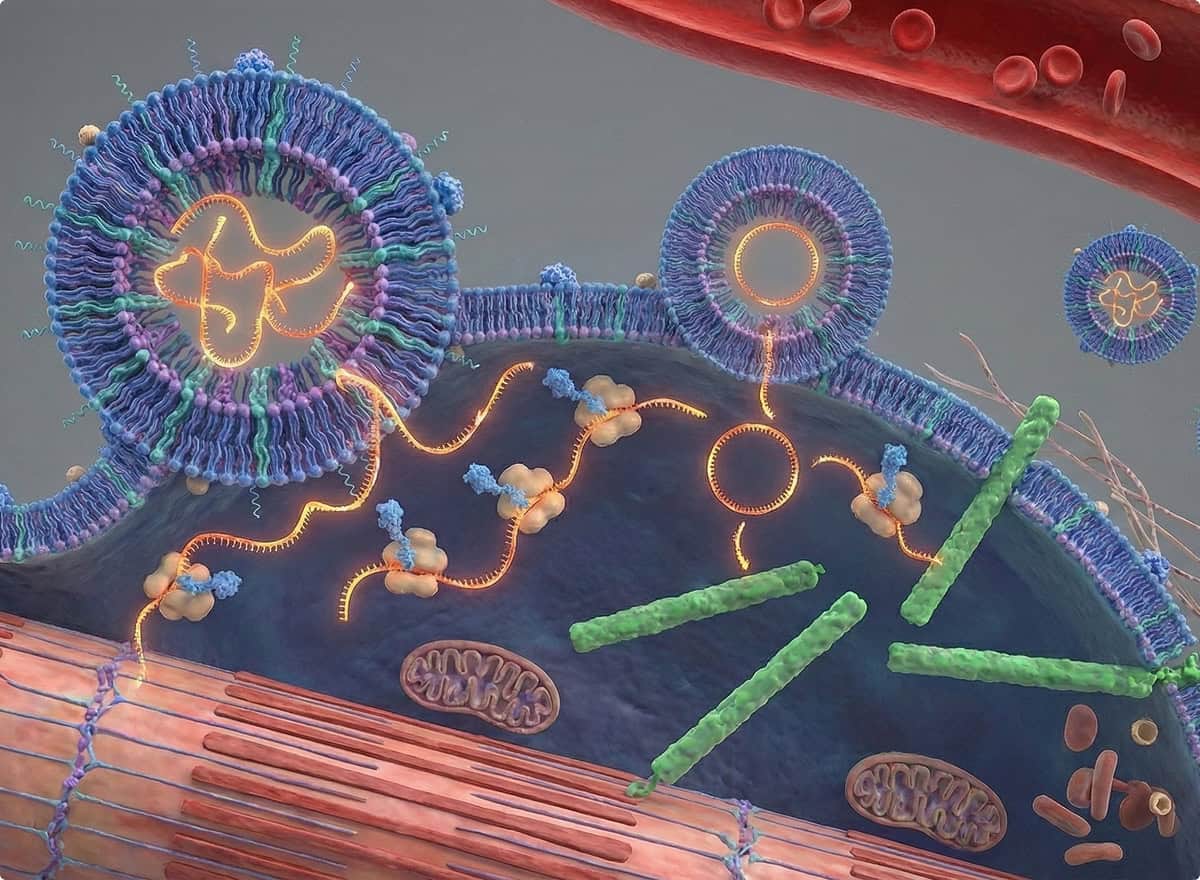
Le programme DMD de LNPureTx vise à restaurer l’expression de la dystrophine — la protéine manquante dans la dystrophie musculaire de Duchenne — grâce à une thérapie à base d’ARNm ou de circRNA encapsulés dans des nanoparticules lipides-polymères de nouvelle génération. Cette approche, non virale, permet de contourner les limites des vecteurs AAV actuellement utilisés (réponses immunitaires, saturation des doses, impossibilité de ré-administration) et ouvre la voie à un traitement répété, flexible et adapté à l’évolution de la maladie.

Les LNP hybrides développés par LNPureTx sont optimisés pour une administration intraveineuse ou intramusculaire, permettant soit une diffusion systémique vers l’ensemble du tissu musculaire, soit une concentration locale dans les zones les plus atteintes. Leur architecture lipide-polymère assure une protection maximale de l’ARNm ou du circRNA, une excellente stabilité dans la circulation sanguine et une délivrance efficace aux fibres musculaires, y compris dans des muscles fragilisés par l’inflammation chronique et la dégénérescence. LNPureTx évalue plusieurs formulations en parallèle afin d’identifier l’option la plus performante pour une expression robuste et durable de la dystrophine.
Les données précliniques in vitro et sur modèles cellulaires dérivés de patients DMD démontrent que les LNP-ARNm et LNP-circRNA testés induisent bien la production de dystrophine fonctionnelle dans les cellules musculaires.
Ces premiers résultats confirment la capacité des nanoparticules à délivrer leur charge génétique au cœur de la fibre musculaire et à rétablir une forme active de la protéine. L’utilisation de circRNA — beaucoup plus stable que l’ARNm classique — ouvre en outre la possibilité d’une expression prolongée, particulièrement adaptée à une maladie nécessitant un apport continu de dystrophine.
Grâce à leur sécurité supérieure, leur absence d’immunogénicité, leur capacité d’encapsulation élevée et leur compatibilité avec les ré-administrations, les LNP de LNPureTx ont le potentiel de transformer la prise en charge de la DMD. L’objectif est clair : offrir une thérapie capable de réintroduire la dystrophine dans le muscle de façon répétée, contrôlée et durable — avec une approche plus sûre, plus stable et plus accessible que les stratégies virales existantes.
En développement
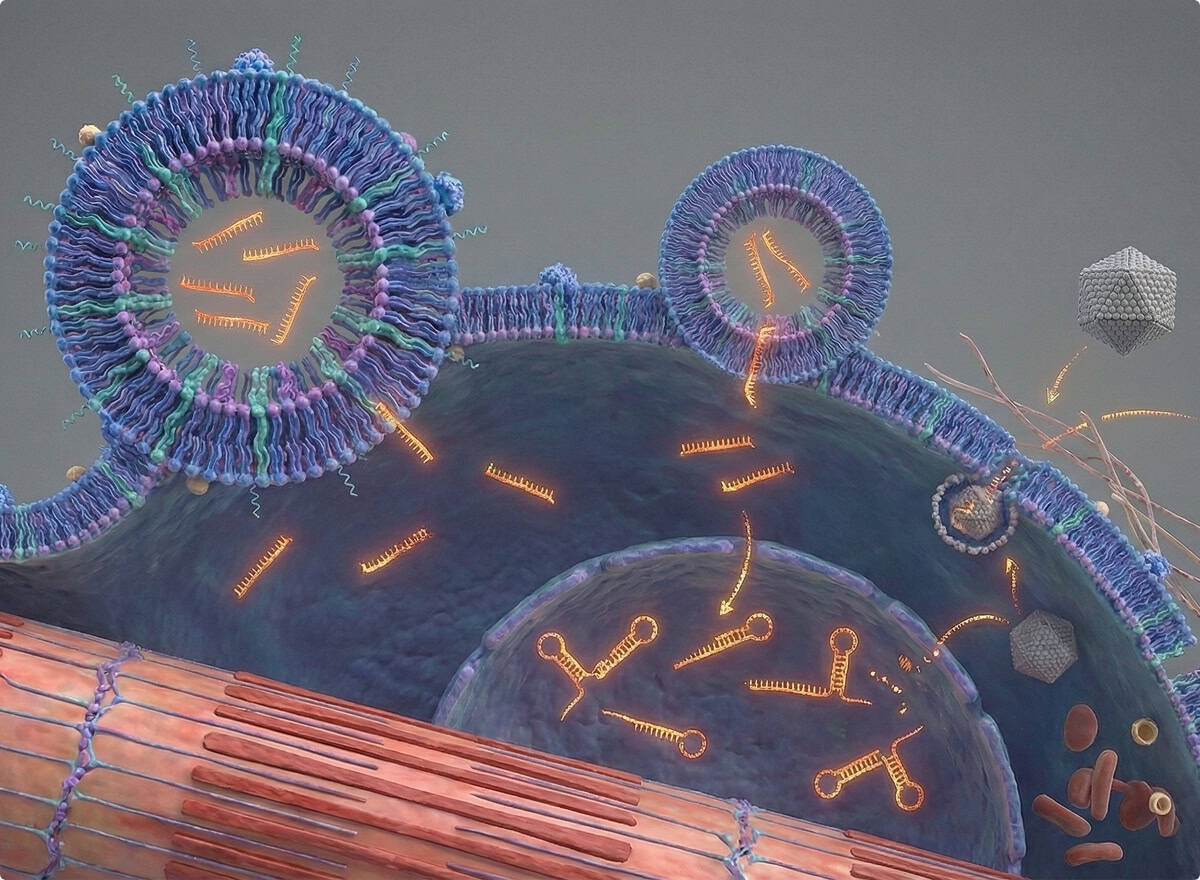
Le programme DM1 de LNPureTx repose sur une innovation majeure : l’utilisation de nanoparticules lipides-polymères (LNP hybrides) pour délivrer au muscle un oligonucléotide antisens (ASO) ciblant directement l’ARN DMPK responsable de la toxicité cellulaire dans la dystrophie myotonique de type 1. Dans la DM1, l’accumulation d’un ARN anormalement répété perturbe l’activité de multiples protéines essentielles au fonctionnement musculaire, cardiaque, nerveux et hormonal. L’objectif de LNPureTx est d’éliminer cette toxicité à la source en réduisant efficacement l’expression de DMPK grâce à une délivrance cellulaire optimisée.

Contrairement aux approches fondées sur les vecteurs AAV, limitées par l’immunogénicité, la faible capacité de charge et l’impossibilité de ré-administrations, la technologie de LNPureTx permet une livraison non virale, sûre et hautement réplicable, adaptée aux besoins d’une thérapie de longue durée contre une maladie multisystémique. Les LNP hybrides développés offrent une protection renforcée de l’ASO, une grande stabilité en milieu biologique et une internalisation très efficace dans les cellules musculaires, y compris les fibres dysfonctionnelles typiques de la DM1.
Les tests précliniques in vitro réalisés sur myoblastes et myotubes dérivés de patients montrent une transfection remarquable, surpassant nettement les performances observées avec des vecteurs AAV dans des conditions comparables.
Cette efficacité se traduit par une réduction significative du transcrit toxique DMPK, accompagnée d’une amélioration des biomarqueurs associés à la restauration des fonctions musculaires et cellulaires essentielles. La diminution du taux d’ARN DMPK est l’un des leviers thérapeutiques les plus prometteurs pour atténuer les symptômes musculaires, cardiaques et neuromusculaires caractéristiques de la maladie de Steinert.
En combinant une pénétration cellulaire supérieure, une sécurité optimale, une technologie non virale et la possibilité d’administrations répétées, les LNP-ASO de LNPureTx ouvrent la voie à une nouvelle génération de thérapies pour la DM1. Cette approche vise à proposer une solution plus efficace, plus stable et plus flexible que les stratégies virales